Chuẩn độ axit – bazơ là kĩ thuật phân tích cho phép xác định nồng độ của dung dịch axit hoặc dung dịch bazơ dựa trên phản ứng trung hòa giữa dung dịch chuẩn (đã biết nồng độ) với một thể tích xác định của dung dịch cần chuẩn độ. Điểm tương đương của chuẩn độ là điểm mà dung dịch chuẩn phản ứng vừa hết với dung dịch cần chuẩn độ. Trong chuẩn độ axit – bazơ, điểm này thường được đánh dấu bằng các chất chỉ thị có khoảng pH đổi màu trùng hoặc rất sát với pH tại điểm tương đương; điểm mà chất chỉ thị thực sự thay đổi màu sắc được gọi là điểm cuối.
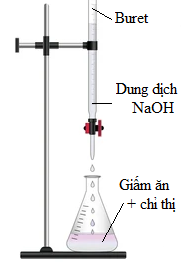
Để xác định lại nồng độ của axit CH3COOH trong mẫu giấm ăn (có nồng độ khoảng 4%; khối lượng riêng D = 1,050 g.ml-1) người ta pha loãng 10,00 ml giấm ăn trên bằng nước cất được 100,00 ml dung dịch X rồi chuẩn độ 10,00 ml dung dịch X bằng dung dịch NaOH chuẩn với chỉ thị thích hợp. Việc chuẩn độ được lặp lại 3 lần.
a) Viết phương trình của phản ứng chuẩn độ (dạng phân tử và ion thu gọn).
b) Vì sao phải thực hiện chuẩn độ nhiều lần?
c) Trong phòng thí nghiệm có các dung dịch NaOH chuẩn với nồng độ như sau: NaOH 1,00M; NaOH 0,05M; NaOH 0,02M. Để thực hiện phép chuẩn độ, sử dụng dung dịch NaOH chuẩn nào là hợp lí nhất? Vì sao? Cho biết buret sử dụng để đựng chất chuẩn trong thí nghiệm này là loại có dung tích 25 ml.
d) Kết quả chuẩn độ 10 ml dung dịch X khi sử dụng dung dịch chuẩn NaOH 0,05M như sau:
……………………….Lần 1… Lần 2… Lần 3
VddNaOH (ml)…. 15,0…. 15,1…. 14,9
Tính nồng độ phần trăm của CH3COOH trong mẫu giấm ăn trên. Chấp nhận các thành phần khác trong mẫu không ảnh hưởng đến kết quả chuẩn độ.
e) Có thể dùng chất chỉ thị nào trong số các chỉ thị được cho trong bảng sau trong phép chuẩn độ trên? Giải thích ngắn gọn (không cần tính toán). Nêu sự đổi màu của dung dịch tại điểm cuối chuẩn độ tương ứng khi sử dụng chỉ thị đó.
Chỉ thị…….. pH đổi màu……. Dạng axit…….. Dạng bazơ
Metyl da cam.. 4,4……………….. Đỏ…………….. Vàng
Phenolphtalein.. 9,0…………. Không màu………… Hồng
Câu trả lời tốt nhất
a. Phản ứng:
CH3COOH + NaOH → CH3COONa + H2O
CH3COOH + OH- → CH3COO- + H2O
b. Phải thực hiện chuẩn độ nhiều lần để tăng độ chính xác cho kết quả chuẩn độ.
c. Ước lượng thể tích dung dịch NaOH:
C%CH3COOH khoảng 4% thì CM = 10D.C%/M = 10.1,05.4/60 = 0,7M
Sau khi đã pha loãng 10 lần thì nồng độ mol/l giảm 10 lần —> Dung dịch X chứa CH3COOH khoảng 0,07M
Vậy 10 ml X chứa nCH3COOH khoảng = 0,07.0,01 = 0,0007
Nếu dùng dung dịch NaOH 1M:
VddNaOH = 0,0007/1 = 0,0007 lít = 0,7 ml: Thể tích quá nhỏ sẽ dẫn đến sai số quá lớn.
Nếu dùng dung dịch NaOH 0,02M:
VddNaOH = 0,0007/0,02 = 0,035 lít = 35 ml: Vượt quá thể tích của buret hiện có (25 ml)
Nếu dùng dung dịch NaOH 0,05M:
VddNaOH = 0,0007/0,05 = 0,014 lít = 14 ml: Phù hợp với buret hiện có, cũng không quá nhỏ để gây ra sai số lớn. Đây là dung dịch phù hợp nhất.
d.
V trung bình = (15 + 15,1 + 14,9)/3 = 15 ml = 0,015 lít
—> nCH3COOH = nNaOH = 0,015.0,05 = 7,5.10^-4
C%CH3COOH = 7,5.10^-4.60.10/10.1,05 = 4,29%
e.
Tại điểm tương đương chất tan trong dung dịch là CH3COONa có môi trường kiềm nên phải chọn chất chỉ thị đổi màu trong môi trường kiềm —> Chọn phenolphtalein.
Dừng chuẩn độ khi dung dịch không màu chuyển sang màu hồng.
tương tự nếu dùng methyl da cam ở bài trên thì ban đầu có màu đỏ, sau đó đến điểm tương đương chuyển sang màu vàng ạ ?
cho e hỏi giả sử chuẩn độ bazo thì dùng phenolphtalein. Ban đầu có màu hồng sau đó đến thời điểm tương đương phenolphtalein mất màu được k ạ ?
