Điện phân 500 ml dung dịch gồm NaCl, HCl và CuSO4 0,02M với điện cực trơ và màng ngăn xốp. Cường độ dòng điện là 2,5A; Coi thể tích dung dịch không thay đổi trong quá trình điện phân. Chỉ số pH theo thời gian được biểu diễn bằng đồ thị sau đây.
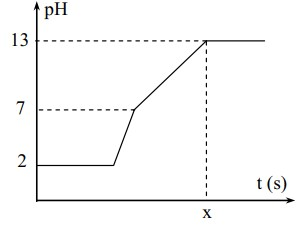
Giá trị của x trong hình vẽ là:
A. 2702 B. 2509
C. 2316 D. 2895
Câu trả lời tốt nhất
Ban đầu: pH = 2 —> [H+] = 0,01 —> nHCl = 0,005
Đoạn 1: pH không thay đổi trong khoảng thời gian catot khử Cu2+ và anot oxi hóa Cl-.
ne đoạn 1 = 2nCu2+ = 0,02
Đoạn 2: pH tăng nhanh chóng do H+ bị khử cho tới khi hết tại catot.
ne đoạn 2 = nH+ = 0,005
Đoạn 3: pH tiếp tục tăng, dung dịch chuyển sang môi trường kiềm do H2O bị khử tại catot tạo OH-:
pH = 13 —> [OH-] = 0,1 —> nOH- = 0,05
2H2O + 2e —> 2OH- + H2
—> ne đoạn 3 = nOH- = 0,05
ne tổng 3 đoạn = 0,075 = It/F
—> t = 2895
Cho e hỏi tại sao biết ở đoạn 2 h20 bên anot chưa bị điện phân vậy ạ nếu h+ sinh ra trung hòa 1 phần oh- bên catot thì vãn được chứ ạ vì ph vẫn tăng nhưng tăng ít hơn
