Dung dịch X chứa a mol NaOH và b mol Ba(AlO2)2. Nhỏ từ từ dung dịch H2SO4 2M vào dung dịch X. Sự thay đổi khối lượng kết tủa theo số mol H2SO4 thêm vào được mô tả thông qua đồ thị dưới đây
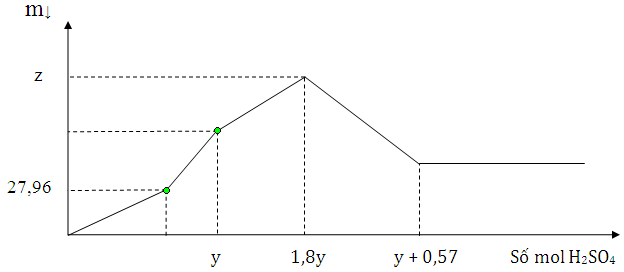
Giá trị của b và z lần lượt là
A. 0,15 và 58,35. B. 0,18 và 70,02.
C. 0,25 và 97,25. D. 0,12 và 46,68.
Câu trả lời tốt nhất
Đoạn 1:
H+ + OH- —> H2O
SO42- + Ba2+ —> BaSO4
nBaSO4 = 0,12 —> nH2SO4 đoạn này = 0,12
—> nNaOH = a = 0,24.
Đoạn 2:
H+ + H2O + AlO2- —> Al(OH)3
SO42- + Ba2+ —> BaSO4
Dễ thấy Ba2+ tham gia phản ứng trước AlO2- nên tại đoạn này Ba2+ sẽ hết.
Vậy b = y (1)
Đoạn 3:
H+ + H2O + AlO2- —> Al(OH)3
Kết thúc đoạn 3 thì nH+ đã dùng = 3,6y và kết tủa Al(OH)3 cực đại.
Vậy: 3,6y = 0,24 + 2b (2)
(1)(2) —> b = y = 0,15
Kết tủa max (z gam) gồm BaSO4 (b) và Al(OH)3 (2b)
—> z = 58,35
Đoạn 4:
3H+ + Al(OH)3 —> Al3+ + 3H2O.
Th ơi sao đoạn 1 không thể ra kết tủa nhôm vậy ạ em đọc rất nhiều bài tương tự nhưng em vẫn chưa hiểu là tại sao nó không ra đồng thời ạ ?
e thắc mắc là sao Ba2+ lại hết ở đọan 2 mà k phải ở đọan 3 ạ?
