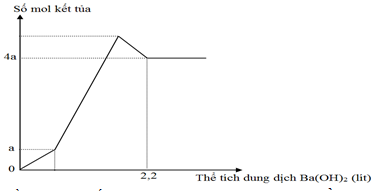
Hòa tan hết 52,56 gam hỗn hợp X gồm Al, Al2O3 và Al(OH)3 trong dung dịch chứa H2SO4 loãng (lấy dư) thu được 1,2a mol khí H2 và dung dịch Y. Cho từ từ Ba(OH)2 1,25M đến dư vào dung dịch Y, phản ứng được biểu diễn theo đồ thị sau:
Phần trăm khối lượng của Al2O3 có giá trị gần nhất với giá trị nào sau đây?
A. 38%. B. 37%. C. 40%. D. 39%.
Câu trả lời tốt nhất
Đoạn 1:
Ba(OH)2 + H2SO4 —> BaSO4 + 2H2O
—> nH2SO4 dư = nBaSO4 đoạn này = a
Sau khi kết tủa Al(OH)3 bị hòa tan hoàn toàn thì chỉ còn lại BaSO4 (4a)
Bảo toàn S —> nAl2(SO4)3 = a
nOH- = nH+ + 4nAl3+ ⇔ 2.2,2.1,25 = 2a + 4.2a
—> a = 0,55
Ban đầu X chứa:
nAl = 2nH2/3 = 0,44; nAl2O3 = x và nAl(OH)3 = y
—> mX = 102x + 78y + 0,44.27 = 52,56
nAl3+ = 2x + y + 0,44 = 2a
—> x = 0,2; y = 0,26
—> %Al2O3 = 38,81%
