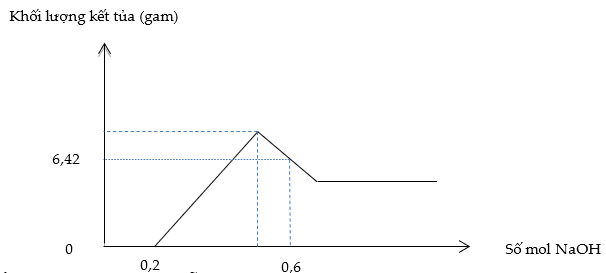
Hòa tan hoàn toàn hỗn hợp X gồm Al và Mg trong 680ml dung dịch HNO3 1M thu được dung dịch Y và khí NO (sản phẩm khử duy nhất). Cho từ từ dung dịch NaOH vào dung dịch Y, lượng kết tủa tạo thành được biểu diễn theo đồ thị sau:
Phần trăm khối lượng của Al trong hỗn hợp đầu là?
A. 63,24% B. 72,79% C. 78,95% D. 53,06%
Câu trả lời tốt nhất
Khi nOH- = 0,2 thì kết tủa mới xuất hiện nên nH+ dư = 0,2
nHNO3 ban đầu = 0,68 —> nH+ phản ứng = 0,48
—> nNO = 0,12
Đặt a, b là số mol Al và Mg
—> 3a + 2b = 0,12.3 (1)
Khi nOH- = 0,6 thì kết tủa gồm Mg(OH)2 (b) và Al(OH)3 (6,42 – 58b)/78
—> 0,6 = 0,2 + 2b + 4a – (6,42 – 58b)/78 (2)
(1)(2) —> a = 0,1 và b = 0,03
—> %Al = 78,95%
×

