Hòa tan m gam hỗn hợp CuSO4 và KCl vào nước thu được dung dịch X. Điện phân dung dịch X với cường độ dòng điện không đổi (điện cực trơ, màng ngăn xốp). Thể tích khí thoát ra (đktc) theo thời gian t được biểu diễn trên đồ thị sau:
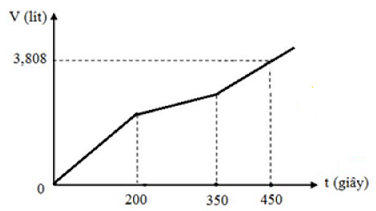
Nếu dừng điện phân ở thời điểm 250 giây rồi đem nhúng thanh nhôm (dư) vào dung dịch, sau phản ứng hoàn toàn, thanh nhôm sẽ:
A. Tăng 1,75g B. Giảm 0,918g
C. Tăng 1,48g D. Giảm 1,25g
Nếu dừng điện phân ở thời điểm 300 giây rồi đem nhúng thanh nhôm (dư) vào dung dịch, sau khi phản ứng hoàn toàn, khối lượng thanh nhôm thay đổi như thế nào?
A. Tăng 0,20 gam. B. Giảm 2,16 gam.
C. Giảm 0,72 gam. D. Tăng 0,92 gam.
Câu trả lời tốt nhất
Đoạn 1: Cu và Cl2
Đoạn 2: Cu và O2 (do độ dốc giảm)
Đoạn 3: H2 và O2
Cứ 100s thì trao đổi x mol electron.
Cu thoát ra hết trong 350s —> nCu = 3,5x/2 = 1,75x
Cl2 thoát ra hết trong 200s —> nCl2 = 2x/2 = x
Khi điện phân 450s:
Catot: nCu = 1,75x —> nH2 = 0,5x
Anot: nCl2 = x —> nO2 = 0,625x
n khí tổng = 0,5x + x + 0,625x = 0,17 —> x = 0,08
Ban đầu: nCuSO4 = 1,75x = 0,14; nKCl = 2x = 0,16
Câu 1.
Khi điện phân 250s thì catot có 0,1 mol Cu và anot có 0,08 mol Cl2 + 0,01 mol O2
—> Dung dịch sau điện phân chứa Cu2+ (0,14 – 0,1 = 0,04), H+ (0,01.4 = 0,04), K+, SO42-
Bảo toàn electron: 3nAl phản ứng = 2nCu2+ + nH+
—> nAl phản ứng = 0,04
Δm = mCu – mAl phản ứng = 0,04.64 – 0,04.27 = 1,48
—> Tăng 1,48 gam
Câu 2.
Khi t = 300 thì ne = 3x = 0,24 —> nCu = 0,12; nCl2 = 0,08; nO2 = 0,02
—> Dung dịch sau điện phân chứa Cu2+ (0,14 – 0,12 = 0,02), H+ (0,02.4 = 0,08), K+, SO42-
Bảo toàn electron: 3nAl phản ứng = 2nCu2+ + nH+
—> nAl phản ứng = 0,04
Δm = mCu – mAl phản ứng = 0,02.64 – 0,04.27 = 0,2
—> Tăng 0,2 gam
Nếu câu 1 (tại tđ 250s) hỏi dd thay đổi như thế nào thì tính ra bao nhiêu ạ?
tại sao chỗ bảo toàn e không phải là 3nAlpu = 2ncu2+ + 2nH+ mà là nH+ thôi ạ
