Monomethylhydrazine (MMH) được sử dụng trong các ứng dụng quân sự làm nhiên liệu đẩy cho tàu vũ trụ và tên lửa. MMH khi tiếp xúc với các chất oxi hoá mạnh (ví dụ: hydrogen peroxide, nitrogen tetroxide, chlorine, fluorine), có thể xảy ra hiện tượng tự bốc cháy.
a) Quá trình Raschig là phương pháp lâu đời nhất để sản xuất hydrazine (N2H4). Ban đầu, ammonia (NH3) trải qua quá trình oxi hoá bởi sodium hypochlorite (NaClO), tạo thành monochloramine (NH4CI) (phản ứng 1). Sau đó, monochloramine phản ứng chậm với ammonia bổ sung trong môi trường kiềm để tổng hợp hydrazine ở nhiệt độ từ 120°C đến 150°C (phản ứng 2). Tuy nhiên, việc tổng hợp hydrazine thông qua quá trình Raschig gặp khó khăn bởi các phản ứng cạnh tranh, đặc biệt là quá trình oxi hoá hydrazine bởi monochloramine (phản ứng 3). Phản ứng phụ này xảy ra với tốc độ nhanh hơn nhiều so với sự hình thành hydrazine.
Quá trình Raschig để tổng hợp monomethylhydrazine (CH3-NH-NH2) là biến thể của phương pháp Raschig truyền thống, người ta sử dụng phản ứng giữa monochloramine với methylamine (CH3NH2) để tạo thành monomethylhydrazine (phản ứng 4). Phản ứng diễn ra trong môi trường kiềm và được kiểm soát nhiệt độ nghiêm ngặt để tối ưu hoá hiệu suất và ngăn chặn sự phân hủy sản phẩm hoặc các phản ứng phụ. Viết các phương trình hoá học các phản ứng từ 1 đến 4.
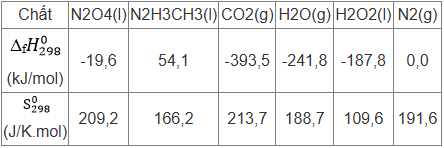
b) Các dữ liệu nhiệt động ở điều kiện chuẩn được cho trong bảng dưới đây:
Tàu con thoi là một hệ thống tàu vũ trụ có thể hoạt động bằng sức đẩy được tạo ra từ quá trình oxi hoá nhiên liệu MMH bởi dinitrogen tetroxide (N2O4) hoặc bởi hydrogen peroxide (H2O2) theo hai phản ứng sau:
5N2O4(l) + 4N2H3CH3(l) → 9N2(g) + 4CO2(g) + 12H2O(g)
5H2O2(l) + N2H3CH3(l) → N2(g) + CO2(g) + 8H2O(g)
i) Hãy tính biến thiên enthalpy chuẩn và biến thiên năng lượng tự do Gibbs của hai phản ứng trên tại nhiệt độ 298K.
ii) Dựa trên nhiệt lượng toả ra từ quá trình oxi hoá 100 gam MMH nhiên liệu (theo tỉ lệ phản ứng) hai phản ứng trên. Hãy cho biết quá trình nào là hiệu quả hơn cho động cơ tàu vũ trụ. Vì sao?
c) Chương trình Artemis của NASA sử dụng oxygen lỏng và hydrogen lỏng làm nhiên liệu. Năng lượng liên kết của H-H là 432 kJ/mol và năng lượng liên kết trung bình của O-H là 460 kJ/mol. Giả thiết sự thay đổi enthalpy cho phản ứng của hydrogen và oxygen ở thể khí là –241 kJ trên mỗi mol khí hydrogen.
i) Tính năng lượng liên kết (theo kJ/mol) của liên kết O=O.
ii) Tính năng lượng tỏa ra (theo kJ) khi đốt cháy 1 dm³ hydrogen lỏng. Biết khối lượng riêng của hydrogen lỏng là 0,071 g/cm³. Biết rằng biến thiên enthalpy (kJ/mol) cho quá trình hoá hơi của hydrogen lỏng và oxygen lỏng lần lượt là 0,9 và 6,8.
(a) Quá trình Raschig truyền thống (Tổng hợp Hydrazine)
(1) Tạo thành monochloramine:
NH3 + NaClO —> NH2Cl + NaOH
(2) Tổng hợp hydrazine:
NH3 + NH2Cl + NaOH —> N2H4 + NaCl + H2O
(3) Phản ứng phụ (Oxi hóa hydrazine bởi monochloramine):
N2H4 + 2NH2Cl —> 2NH4Cl + N2
(4) Tổng hợp monomethylhydrazine (biến thể quá trình Raschig):
CH3NH2 + NH2Cl + NaOH —> CH3-NH-NH2 + NaCl + H2O
(b)

