Một pin điện hóa được lắp đặt như hình bên.
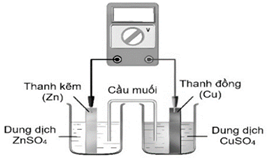
Cầu muối chứa NH4Cl. Cho các phát biểu sau về pin điện hóa trên khi hoạt động:
(a) Thanh kẽm đóng vai trò là cathode còn thanh đồng đóng vai trò là anode.
(b) Khối lượng điện cực Zn giảm còn khối lượng thanh đồng tăng.
(c) Ở mạch ngoài, dòng electron di chuyển từ thanh kẽm đến thanh đồng.
(d) Phản ứng xảy ra trong pin là Zn + Cu2+ → Zn2+ + Cu.
(e) Nồng độ ZnSO4 và CuSO4 ở trong hai dung dịch không thay đổi.
Số phát biểu đúng là
A. 2. B. 3. C. 4. D. 1.
Câu trả lời tốt nhất
(a) Sai, Zn có tính khử mạnh hơn Cu nên thanh Zn là anode, thanh Cu là cathode.
(b) Đúng, khối lượng điện cực Zn giảm do:
Zn —> Zn2+ + 2e
Khối lượng điện cực Cu tăng do:
Cu2+ + 2e —> Cu
(c)(d) Đúng
(e) Sai, nồng độ CuSO4 giảm do Cu2+ đã bị khử và NH4+ từ cầu muối đi tới tạo (NH4)2SO4.
Nồng độ ZnSO4 gần như không đổi, Zn2+ tạo thêm được Cl- từ cầu muối di chuyển tới trung hòa điện tích. Rất ít ion SO42- từ bên kia có thể vượt qua được cầu muối.

