Nguyên tử của nguyên tố X có tổng số hạt cơ bản (proton, electron, neutron) là 24, trong đó tổng số hạt mang điện gấp hai lần tổng số hạt không mang điện.
a) Xác định nguyên tố X. (Cho biết số hiệu nguyên tử của một số nguyên tố: C = 6, N = 7, O = 8, F = 9, Na = 11, Mg = 12)
b) Viết công thức electron, công thức Lewis, công thức cấu tạo của các phân tử: H2X, CX2 (H là nguyên tố hydrogen, C là nguyên tố carbon).
c) Dựa vào cấu trúc phân tử, giải thích tại sao phân tử H2X phân cực, phân tử CX2 không phân cực?
Câu trả lời tốt nhất
(a) Tổng hạt = 2Z + N = 24
Số hạt mang điện (2Z) gấp hai lần tổng số hạt không mang điện (N) —> 2Z = 2N
—> Z = N = 8 —> X là O
(b)(c) Công thức Lewis và dạng hình học của H2O, CO2:
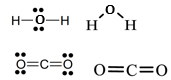
Độ âm điện của O lớn hơn của H nên 2 đôi electron dùng chung lệch về phía O, phân tử H2O dạng góc nên mỗi H dư một phần điện dương (δ+) và O dư một phần điện âm (2δ-) —> Phân tử H2O phân cực.
Độ âm điện của O lớn hơn của C nên các đôi electron dùng chung lệch về phía O, mỗi liên kết C=O có phân cực nhưng phân tử CO2 thẳng hàng nên toàn bộ phân tử lại không phân cực.
