Sục từ từ khí CO2 đến dư vào dung dịch chứa Ba(OH)2 và NaAlO2. Khối lượng kết tủa thu được sau phản ứng được biểu diễn trên đồ thị sau:
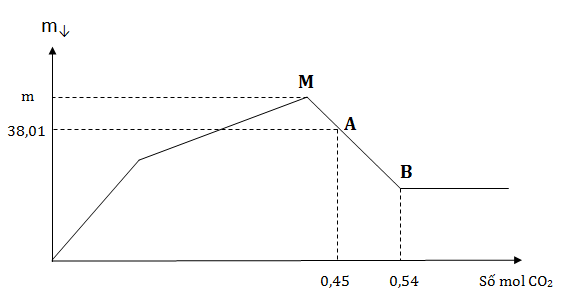
Giá trị của m là:
A. 47,86 B. 57,71 C. 49,05 D. 35,30
Câu trả lời tốt nhất
Ban đầu đặt a, b là số mol Ba(OH)2 và NaAlO2.
Tại điểm B các chất tồn tại ở dạng Ba(HCO3)2 (a mol); NaHCO3 (b mol)
Bảo toàn C —> nCO2 = 2a + b = 0,54 (1)
Tại điểm A:
nNaHCO3 = nAl(OH)3 = b
m↓ = 38,01 —> nBaCO3 = (38,01 – 78b)/197
Bảo toàn Ba —> nBa(HCO3)2 = a – (38,01 – 78b)/197
Bảo toàn C —> (38,01 – 78b)/197 + 2[a – (38,01 – 78b)/197] + b = 0,45 (2)
(1)(2) —> a = 0,14 và b = 0,26
m ↓max = mBaCO3 + mAl(OH)3 = 197a + 78b = 47,86
Đáng ra ở chỗ m phải có một đoạn ngang để hoà tan na2co3 rồi mới đi xuống đúng ko ad
a,b là mol Ba(oh)2 và NaAlo2. Ta có
Tại A: nbaco3 còn lại =0,54-0,45=0,09
=> nAl(OH)3max =b=( 38,01-0,09.197)/78=0,14
Tại B: nCO2=2a+b=0,54 => a=0,26
Giải thích:
Để tạo 1 mol BaCo3 hay Al(oh)3 đều cần 1mol Co2. Để hoà tan 1 mol baco3 cũng cần 1mol co2
Tại M: nco2 =a+b
Tại B: nco2 =2a +b
Tại A: nco2 = a+b+x
Trong đó x là mol baco3 bị hoà tan
sao ở B lại chỉ có Ba(HCo3)2 và NaHCo3 ạ, 2 cái này làm gì có kết tủa ad???

