Trong bình có dung tích không đổi 1 Lít, ban đầu nạp vào bình hỗn hợp gồm 0,9 mol chất A và 0,6 mol chất B. Giữ nhiệt độ ổn định ở 760°C, xảy ra cân bằng hóa học:
aA(g) + bB(g) ⇋ cC(g) + dD(g) (a, b, c, d là các hệ số nguyên, tối giản của phản ứng; biểu thức tính tốc độ phản ứng tuân theo định luật tác dụng khối lượng)
Sau 6 phút, phản ứng đạt tới trạng thái cân bằng. Sự phụ thuộc nồng độ mol/L của các chất trong bình phản ứng vào thời gian (phút) được biểu diễn bằng đồ thị sau:
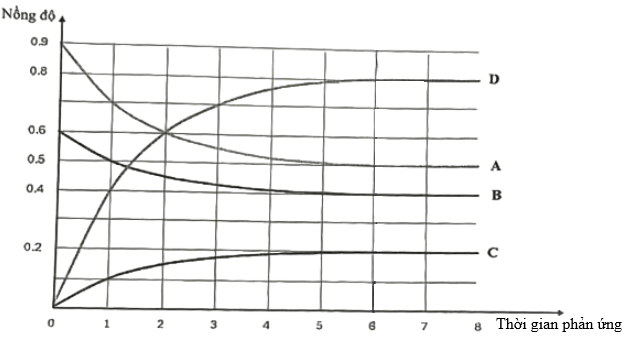
a) Trước khi đạt tới trạng thái cân bằng, tốc độ phản ứng nghịch giảm dần theo thời gian.
b) Ở trạng thái cân bằng, nếu tăng nhiệt độ của bình phản ứng thì số mol khí trong bình tăng lên, chứng tỏ rằng phản ứng thuận là phản ứng tỏa nhiệt.
c) Hằng số cân bằng của phản ứng ở 760°C là 0,8192.
d) Tốc độ trung bình của phản ứng thuận trong khoảng thời gian từ 0 đến 6 phút là 1/1800 mol/Ls
Câu trả lời tốt nhất
(a) Sai, trước khi đạt tới trạng thái cân bằng thì nồng độ C, D đều tăng nên tốc độ phản ứng nghịch tăng dần theo thời gian.
(b) Sai:
aA(g) + bB(g) ⇋ cC(g) + dD(g)
0,9………0,6………..0………0
xa………..xb……….xc…….xd
0,5……….0,4……..0,2…….0,8
—> xa = 0,4; xb = 0,2; xc = 0,2 và xd = 0,8
—> a : b : c : d = 0,4 : 0,2 : 0,2 : 0,8 = 2 : 1 : 1 : 4
—> a = 2; b = 1; c = 1; d = 4
Nếu tăng nhiệt độ của bình phản ứng thì số mol khí trong bình tăng lên —> Cân bằng chuyển dịch theo chiều thuận (do c + d > a + b) —> Chiều thuận thu nhiệt.
(c) Đúng
Kc = 0,2.0,8^4/(0,5².0,4) = 0,8192
(d) Đúng
v thuận = -½.(0,5 – 0,9)/360 = 1/1800 mol/Ls
