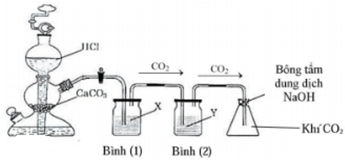
Trong sơ đồ trên ở bình nón, kỹ thuật viên cho vào đó 200 ml dung dịch chứa Ca(OH)2 bão hòa (d = 1,02 g/ml) ở 25°C. Sau một thời gian sục khí CO2, lấy bình ra, lọc bỏ phần kết tủa và cân lại phần dung dịch (sau khi đã trừ khối lượng bình) thấy khối lượng dung dịch sau phản ứng giảm 0,2 gam. Thêm tiếp NaOH dư vào bình sau phản ứng thì có kết tủa xuất hiện. Tính khối lượng kết tủa thu được thêm.
Nếu giả sử hiệu suất hấp thụ khí CO2 vào dd Ca(OH)2 là 70% thì thể tích CO2 (đkc) điều chế được trong thí nghiệm trên là bao nhiêu?
Biết độ tan của Ca(OH)2 trong nước ở 25°C là 0,17g/100 g nước. Giả thiết lượng thể tích chất rắn dùng điều chế Ca(OH)2 bão hòa không đáng kể.
Câu trả lời tốt nhất
mCa(OH)2 = 200.1,02.0,17/(100 + 0,17) = 0,346211441 gam
—> nCa(OH)2 = 0,0046785
CO2 + Ca(OH)2 —> CaCO3 + H2O
x…………..x……………….x
2CO2 + Ca(OH)2 —> Ca(HCO3)2
2y……………y………………..y
nCa(OH)2 = x + y = 0,0046785
Δmdd = 44(x + 2y) – 100x = -0,2
—> x = 0,004248; y = 0,000431
Ca(HCO3)2 + 2NaOH —> CaCO3 + Na2CO3 + 2H2O
nCaCO3 thu thêm = y —> mCaCO3 thu thêm = 0,0431 gam
V CO2 = 24,79(x + 2y)/70% = 0,180967 L
