Một nhóm học sinh tiến hành thí nghiệm điện phân 200 mL dung dịch CuSO4 0,5M, sử dụng bộ dung cụ được mô tả như hình bên. Giả thiết quá trình điện phân duy trì ở 30 – 35°C; hiệu điện thế được giữ cố định; giá trị pH của dung dịch điện phân được giữ ổn định; không xảy ra quá trình điện phân nước bỏ qua sự bay hơi của nước trong quá trình điện phân.
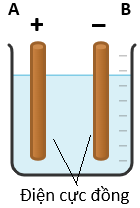
a) Cho biết vai trò (cathode và anode) của điện cực Cu (A) và điện cực Cu (B).
b) Sau một thời gian điện phân, khối lượng điện cực Cu (A) và khối lượng điện cực Cu (B) tăng, giảm hay không đổi? Giải thích.
c) Trong công nghiệp, người ta tinh luyện đồng (Cu, copper) bằng phương pháp điện phân. Đồng có độ tinh khiết cao có thể thu được từ đồng phế liệu hoặc đồng thô (có độ tinh khiết thấp). Hai tấm kim loại đồng gồm: đồng có độ tinh khiết cao và đồng phế liệu được sử dụng làm hai điện cực. Kết thúc quá trình điện phân, đồng tinh khiết được thu hồi ở điện cực cathode hay điện cực anode?
d) Trong thực tế, mạ đồng từ dung dịch copper(II) sulfate người ta thường chú ý sự ảnh hưởng của ion Cu2+ đến quá trình mạ và chất lượng lớp kim loại mạ. Ion Cu+ sinh ra do phản ứng thuận nghịch của kim loại Cu khử ion Cu2+ trong dung dịch (phản ứng 1). Khi dung dịch không có acid, Cu+ ở dạng muối sulfate sẽ bị thủy phân tạo ra copper(I) oxide (phản ứng 2) ở dạng rắn, lơ lửng trong dung dịch. Vì vậy, người ta phải thêm dung dịch sulfuric acid vào dung dịch mạ và khuấy bằng không khí nén, tạo điều kiện để oxy hóa copper(I) oxide (phản ứng 3) và oxy hóa copper(I) sulfate (phản ứng 4) thành copper(II) sulfate. Viết phương trình hóa học các phản ứng từ 1 đến 4.
Câu 2. Một học sinh tiến hành thí nghiệm điện phân 100 mL dung dịch CuSO4 0,5M, sử dụng bộ dụng cụ được mô tả như hình bên.

Cho biết trong thí nghiệm: hiệu điện thế được giữ cố định, đảm bảo nước không bị điện phân ở cả hai điện cực, bỏ qua sự bay hơi của nước trong quá trình điện phân. Cho các phát biểu sau:
a) Giá trị pH của dung dịch sẽ tăng dần trong quá trình điện phân.
b) Sau một thời gian điện phân nồng độ dung dịch CuSO4 giảm.
c) Sau một thời gian điện phân, điện cực Cu (B) có khối lượng tăng lên.
d) Nếu thay 100 mL dung dịch CuSO4 0,5M bằng 100 mL dung dịch CuSO4 có nồng độ nhỏ hơn 0,5M thì tốc độ điện phân sẽ tăng.
Câu trả lời tốt nhất
(a) Điện cực Cu (A) nối với cực dương của nguồn điện, đóng vai trò là anode.
Điện cực Cu (B) nối với cực âm của nguồn điện, đóng vai trò là cathode.
(b) Điện cực Cu (A) có khối lượng giảm vì bị tan ra:
Cu —> Cu2+ + 2e
Điện cực Cu (B) có khối lượng tăng vì có Cu mới bám vào:
Cu2+ + 2e —> Cu
(c) Đồng phế liệu hoặc đồng thô (có độ tinh khiết thấp) dùng làm anode. Đồng có độ tinh khiết cao dùng làm cathode.
Kết thúc quá trình điện phân, đồng tinh khiết được thu hồi ở điện cực cathode (như mô hình trên).
(d) Các phản ứng:
(1) Cu + CuSO4 ⇋ Cu2SO4
(2) Cu2SO4 + H2O ⇋ Cu2O + H2SO4
(3) 2Cu2O + O2 + 4H2SO4 —> 4CuSO4 + 4H2O
(4) 2Cu2SO4 + O2 + 2H2SO4 —> 4CuSO4 + 2H2O
Câu 2.
(a)(b) Sai, pH của dung dịch không thay đổi do nồng độ Cu2+ không đổi:
(A) Cu —> Cu2+ + 2e
(B) Cu2+ + 2e —> Cu
(c) Đúng, sau một thời gian điện phân, điện cực Cu (B) có khối lượng tăng lên do Cu2+ bị khử thành Cu bám vào.
(d) Sai, khi dung dịch loãng hơn thì điện trở tăng, hiệu điện thế được giữ cố định nên cường độ dòng điện giảm —> Tốc độ điện phân giảm.

