Al2O3 có nhiệt độ nóng chảy rất cao (2050°C) nên việc điện phân nóng chảy Al2O3 nguyên chất sẽ khó thực hiện. Hiện nay, theo công nghệ Hall-Héroult, người ta hoà tan Al2O3 trong cryolite (Na3AlF6) nóng chảy được hỗn hợp chất điện phân có nhiệt độ nóng chảy thấp hơn (khoảng gần 1000°C). Giải pháp này giúp tiết kiệm năng lượng, đồng thời tạo ra chất lỏng có tính dẫn điện tốt, nhẹ hơn Al và nổi lên phía trên lớp Al lỏng, bảo vệ Al không bị oxi hoá bởi không khí. Sơ đồ thùng điện phân được biểu diễn như hình dưới:
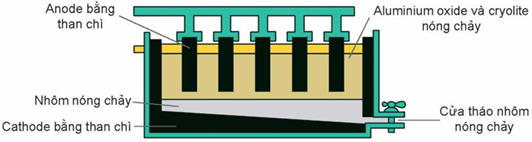
Quá trình điện phân được tiến hành với dòng điện có hiệu điện thế thấp (khoảng 5 V) và cường độ dòng điện 100 – 300 kA. Để sản xuất được 1 tấn Al cần tiêu tốn khoảng 2 tấn Al2O3, 50 kg cryolite, 400 kg than cốc. Cho biết: Năng lượng điện tiêu thụ theo lí thuyết, Alt = (U.mAl. F)/(9.3,6.10⁶)(kWh). Với: mAl là khối lượng Al được điều chế (gam); F là hằng số Faraday, F = 96485 C/mol; U (V) là hiệu điện thế áp đặt vào hai cực của bình điện phân.
a) Với hiệu điện thế thấp (khoảng 5 V), cryolite không bị điện phân.
b) Tại cathode và anode lần lượt xảy ra quá trình oxi hoá cation Al3+ và khử anion O2-.
c) Tiến hành điện phân Al2O3 (hiệu suất điện phân 100%), ở anode thu được 74,37 m³ (đkc) hỗn hợp khí X có tỉ khối so với hydrogen bằng 16. Lấy 2,479 lít (đkc) hỗn hợp khí X sục vào dung dịch nước vôi trong (dư) thu được 2 gam kết tủa thì khối lượng Al thu được ở cathode là 90,5 kg.
d) Năng lượng điện tiêu thụ để sản xuất được 1,5 kg Al theo lí thuyết là 22,3345 kWh.
Câu trả lời tốt nhất
(a) Sai, ngoài vai trò vật lý (hạ nhiệt độ nóng chảy của Al2O3, tăng tính dẫn điện của chất điện phân nóng chảy, tạo lớp bảo vệ nhôm nóng chảy) cryolite còn đóng vai trò chất xúc tác. Với vai trò hóa học này, đương nhiên cryolite có tham gia vào các quá trình điện phân.
Tham khảo cơ chế xúc tác của cryolite (Na3AlF6 hay 3NaF.AlF3):
+ NaF bị điện phân: 2NaF —> 2Na + F2
+ Na khử Al3+ và tái tạo NaF: 3Na + AlF3 —> 3NaF + Al
+ F2 khử O2- và tái tạo AlF3: 6F2 + 2Al2O3 —> 4AlF3 + 3O2
Cryolite không bị hao hụt bởi phản ứng (như mọi chất xúc tác khác) nhưng nó vẫn bị thất thoát nên cần bổ sung định kỳ như một dạng nguyên liệu.
(b) Sai, ngoài các quá trình tạo Al, O2 theo cách trên, Al3+ vẫn bị khử tại cathode và O2- vẫn bị oxi hóa tại anode.
(c) Sai
0,1 mol X chứa nCO2 = nCaCO3 = 0,02; nCO = x và nO2 = y
—> x + y + 0,02 = 0,1
mX = 28x + 32y + 0,02.44 = 0,1.2.16
—> x = 0,06; y = 0,02
Bảo toàn electron: 3nAl = 4nCO2 + 2nCO + 4nO2
—> nAl = 7/75 —> mAl = 2,52 gam
Tỉ lệ: 2,479 L X tương ứng có 2,52 gam Al tạo ra
—> 74,37 m³ X tương ứng mAl = 74,37.2,52/2,479 = 75,6 kg Al
(d) Đúng: Alt = 5.1500.96485/(9.3,6.10⁶) = 22,3345 kWh.
