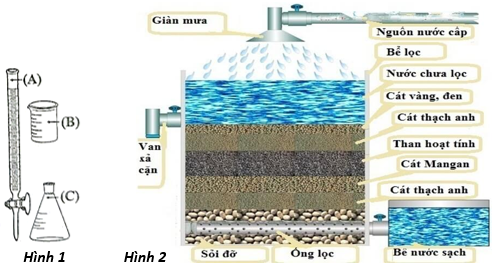
Để sử dụng nước sinh hoạt ở vùng nước nhiểm sắt ở một số vùng, người ta sử dụng hệ thống lọc nước kiểu giàn mưa như hình 2. Một nhóm học sinh tìm hiểu ảnh hưởng của giàn mưa ảnh hưởng đến nồng độ ion Fe2+ trong nước giếng khoan nhiễm sắt. Giả thuyết của nhóm học sinh là: “nước giếng khoan sau khi đi qua hệ thống lọc nước kiểu giàn mưa, nồng độ Fe2+ giảm”. Nhóm học sinh chuẩn bị:
+ 100,0 mL nước giếng khoan vừa bơm lên đựng trong cốc thủy tinh lớn (dán nhãn cốc là Y)
+ 100,0 mL nước giếng khoan sau khi đi qua hệ thống lọc trong cốc thủy tinh (dán nhãn cốc là Z)
Nhóm tiến hành các thí nghiệm như sau:
– Chuẩn độ Fe2+ trong nước vừa lấy từ giếng khoan (cốc Y):
• Bước 1: Lấy 10,00 mL dung dịch trong bình Y cho vào bình tam giác rồi thêm tiếp 5 mL dung dịch H2SO4 2 M.
• Bước 2: Chuẩn độ dung dịch trong bình tam giác bằng dung dịch KMnO4 2,20×10⁻² M đến khi xuất hiện màu hồng nhạt (bền trong khoảng 20 giây) thì dừng. Ghi lại thể tích dung dịch KMnO4 đã dùng.
Lặp lại thí nghiệm chuẩn độ thêm 2 lần. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 10,40 mL. Nồng độ của Fe(II) xác định được là C1 M.
– Chuẩn độ Fe2+ trong nước sau khi lọc (cốc Z):
Xác định hàm lượng Fe(II) của dung dịch chứa trong bình Z theo các bước tương tự như lần thứ nhất. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 2,43 mL. Nồng độ của Fe(II) xác định được là C2 M.
Nồng độ dung dịch KMnO4 như nhau trong các thí nghiệm chuẩn độ. Sự thay đổi nồng độ của Fe(II) (q%) được tính theo công thức: q = (C1 – C2)/C1. Giả thiết các ion khác trong nước không ảnh hưởng đến phản ứng của Fe2+ với KMnO4/H2SO4.
a) Khi chuẩn độ, dung dịch KMnO4 được nhỏ trực tiếp vào bình tam giác từ dụng cụ kí hiệu là (B) được minh họa ở Hình 1.
b) Giá trị của q là 76,6. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười. ).
c) Giá trị của C2 là 0,003. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần nghìn. ).
d) Kết quả thu được từ các thí nghiệm phù hợp với giả thuyết ban đầu của nhóm học sinh.
Câu trả lời tốt nhất
(a) Sai, chuẩn độ phải nhỏ chậm và dừng đúng lúc (nhất là khi gần điểm kết thúc), cốc thủy tinh B không đảm bảo độ chính xác (do mặt thoáng quá lớn), cũng không thể dừng đúng lúc. Vì vậy phải dùng burrete A để chuẩn độ.
(b) Đúng (c) Sai:
Phản ứng chuẩn độ:
5Fe2+ + MnO4- + 8H+ —> 5Fe3+ + Mn2+ + 4H2O
– Chuẩn độ Fe2+ trong Y:
nMnO4- = 2,2.10^-2.10,4 = 0,2288 mmol
—> C1 = 0,2288.5/10 = 0,1144 M
– Chuẩn độ Fe2+ trong Z:
nMnO4- = 2,2.10^-2.2,43 = 0,05346 mmol
—> C2 = 0,05346.5/10 = 0,02673 M (làm tròn thành 0,027)
q = (C1 – C2)/C1 = 76,6%
(d) Đúng, nước giếng khoan sau khi đi qua hệ thống lọc nước kiểu giàn mưa, nồng độ Fe2+ giảm do Fe2+ bị oxi hóa, chuyển thành kết tủa và bị các lớp lọc giữ lại.
