Điện phân dung dịch X chứa Cu(NO3)2 và NaCl với điện cực trơ thấy thể tích khí thoát ra ở các điện cực (V lít ở đktc) và thời gian điện phân (t giây) phụ thuộc nhau như trên đồ thị sau:
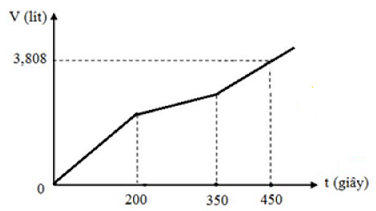
Nếu dừng điện phân ở thời điểm 300 giây thu được dung dịch Y. Cho dung dịch Y tác dụng với lượng Fe dư (NO là sản phẩm khử duy nhất của N+5) thì lượng Fe tối đa đã phản ứng có giá trị là
A. 1,40 gam. B. 3,08 gam.
C. 2,80 gam. D. 1,68 gam.
Câu trả lời tốt nhất
Đoạn 1: Cu và Cl2
Đoạn 2: Cu và O2 (do độ dốc giảm)
Đoạn 3: H2 và O2
Cứ 100s thì trao đổi x mol electron.
Cu thoát ra hết trong 350s —> nCu = 3,5x/2 = 1,75x
Cl2 thoát ra hết trong 200s —> nCl2 = 2x/2 = x
Khi điện phân 450s:
Catot: nCu = 1,75x —> nH2 = 0,5x
Anot: nCl2 = x —> nO2 = 0,625x
n khí tổng = 0,5x + x + 0,625x = 0,17 —> x = 0,08
Ban đầu: nCu(NO3)2 = 1,75x = 0,14; nNaCl = 2x = 0,16
Khi t = 300 thì ne = 3x = 0,24 —> nCu = 0,12; nCl2 = 0,08; nO2 = 0,02
—> Dung dịch sau điện phân chứa Cu2+ (0,14 – 0,12 = 0,02), H+ (0,02.4 = 0,08), Na+, NO3-
nNO = nH+/4 = 0,02; lượng sắt tối đa nên tạo Fe2+.
Bảo toàn electron: 2nFe phản ứng = 2nCu2+ + 3nNO
—> nFe phản ứng = 0,05 —> mFe = 2,80 gam
