Hòa tan hoàn toàn hỗn hợp gồm Na, Ba và Al2O3 vào nước dư, thu được 3,136 lít khí H2 (đktc) và dung dịch X chỉ chứa hai muối gồm NaAlO2 và Ba(AlO2)2. Cho dung dịch H2SO4 đến dư vào X, sự phụ thuộc khối lượng kết tủa (gam) với số mol H2SO4 được biểu diễn theo đồ thị sau:
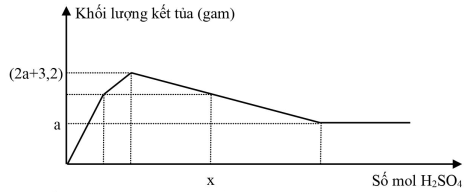
Giá trị của x là
A. 0,30. B. 0,36. C. 0,34. D. 0,32.
Câu trả lời tốt nhất
Đoạn 1:
Ba2+ + SO42- —> BaSO4
AlO2- + H+ + H2O —> Al(OH)3
Đặt nBa(AlO2)2 = b —> nBaSO4 = b và nAl(OH)3 = 2b
—> m↓ khi kết thúc đoạn 1 là 389b
Đoạn 2:
AlO2- + H+ + H2O —> Al(OH)3
Khi kết thúc đoạn 2 thì mBaSO4 = a = 233b
Đoạn 2 đã tạo thêm mAl(OH)3 = 2a + 3,2 – 389b = 77b + 3,2
—> nNaAlO2 = nAl(OH)3 đoạn 2 = (77b + 3,2)/78
Bảo toàn electron:
nNa + 2nBa = 2nH2
⇔ (77b + 3,2)/78 + 2b = 0,14.2 —> b = 0,08
Đoạn 3:
Al(OH)3 + 3H+ —> Al3+ + 3H2O
Tại vị trí đang xét (nH2SO4 = x) thì kết tủa thu được giống như đoạn 1 —> Toàn bộ lượng Al(OH)3 tạo ra ở đoạn 2 đã tan trở lại.
—> nH+ = 2b + 4(77b + 3,2)/78 = 0,64
—> nH2SO4 = x = 0,32.
