Một nhóm học sinh tiến hành thí nghiệm điện phân điều chế chlorine và so sánh tính oxy hóa của chlorine với iodine như sau: Cho vào bình điện phân (có màng ngăn xốp) 300 mL dung dịch hỗn hợp NaCl 2M, KI 2M và vài giọt dung dịch hồ tinh bột, nối bình điện phân với nguồn điện một chiều (như hình vẽ bên).
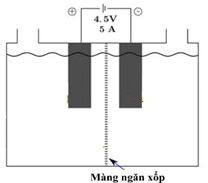
Nhóm học sinh trên tiến hành điện phân trong thời gian 30 phút với cường độ không đổi là 5 A thấy phần dung dịch bên phía anode chuyển sang màu xanh. Biết số mol electron đi qua dây dẫn được tính bằng công thức: n = I.t/96500, trong đó: I là cường độ dòng điện (A), t là thời gian (giây).
Sau khi tra cứu được các giá trị thế điện cực chuẩn E°Cl2/2Cl- = 1,36V; E°I2/2I- = 0,54V, nhóm học sinh đưa ra nhận định “Trong quá trình điện phân trên, ở anode chỉ có ion Cl- bị oxi hóa thành Cl2, Cl2 phản ứng với dung dịch KI tạo ra I2 làm xanh hồ tinh bột”.
a) Phần dung dịch bên phía anode chuyển sang màu xanh chứng tỏ có I2 sinh ra và nhận định của nhóm học sinh trên là đúng.
b) Nếu cho phenolphthalein vào phần dung dịch bên phía cathode, dung dịch sẽ chuyển thành màu hồng.
c) Sau khi điện phân, nếu tháo màng ngăn, khuấy đều dung dịch sẽ tạo thành nước Javel.
d) Sau điện phân, nhóm học sinh trên lấy 5 mL dung dịch bên anode đem pha loãng bằng nước cất và chuẩn độ bằng dung dịch Na2S2O3 0,1 M đến khi dung dịch mất màu thì dùng hết 29,8 mL. Biết phương trình chuẩn độ: 2Na2S2O3 + I2 → Na2S4O6 + 2NaI. Nồng độ mol/L của I2 được xác định bằng phương pháp chuẩn độ trên là 0,298M. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần nghìn).
Câu trả lời tốt nhất
(a) Sai, tại anode có Cl-, I-, H2O.
E°Cl2/2Cl- > E°I2/2I- chứng tỏ I- có tính khử mạnh hơn Cl- và I- trực tiếp bị oxi hóa tại anode thành I2, do đó nhận định trên là không đúng.
Chú ý: Ban đầu Cl- và I- cùng nồng độ, rõ ràng I- mạnh mẽ hơn và chiếm suất điện phân trước. Tới lúc nào đó nồng độ I- giảm dần, Cl- nhờ ưu thế nồng độ sẽ bắt đầu bị điện phân. Vì vậy Cl2 oxi hóa I- là có xảy ra, nhận định sai vì khẳng định “chỉ có ion Cl- bị oxi hóa”.
(b) Đúng, tại cathode xuất hiện OH- làm phenolphthalein chuyển sang màu hồng:
2H2O + 2e —> 2OH- + H2
(c) Sai, với bình điện phân như vậy thì Cl2 (nếu có, xuất hiện sau khi I- đã giảm tới mức nào đó) cũng đã thoát ra ngoài nên kết thúc điện phân mới tháo màng ngăn thì không còn đủ Cl2 để tạo nước Javel nữa.
(d) Đúng:
nNa2S2O3 = 2,98 mmol —> nI2 = 1,49 mmol
—> CM I2 = 1,49/5 = 0,298M
