Vào năm 1780, Luigi Galvani phát hiện ra rằng khi hai kim loại khác nhau (ví dụ đồng và kẽm) được kết nối và sau đó cả hai cùng chạm vào hai phần khác nhau của dây thần kinh của một con ếch, thì chân con ếch co rút. Ông gọi đây là “điện động vật”. Một pin Galvani được tạo nên từ hai cặp oxi hoá – khử khác nhau ví dụ Sn2+/Sn và Zn2+/Zn. Biết: E°Sn2+/Sn = -0,13V; E°Zn2+/Zn = -0,76V.
a) Mô tả cấu tạo Pin X được tạo nên khi ghép nối với nhau hai điện cực chuẩn trên. Hãy vẽ sơ đồ cấu tạo của pin X và chỉ rõ điện cực dương, điện cực âm và chiều di chuyển của dòng điện.
b) Tính sức điện động chuẩn của pin X.
c) Thực tế khi nồng độ của các muối thay đổi thì thế điện cực của các điện cực cũng thay đổi dẫn đến sức điện động của pin cũng thay đổi theo. Giá trị của thế điện cực kim loại ở điều kiện không chuẩn phụ thuộc vào nồng độ của cation kim loại ở điện cực theo phương trình Nernst:
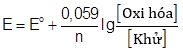
(với n là số electron trao đổi ở điện cực). Hãy tính tỉ lệ nồng độ của Zn2+ so với nồng độ Sn2+ ở điện cực khi pin X hết điện.
d) Một học sinh nêu giả thuyết: “Có thể tạo được pin Galvani từ hai điện cực của cùng một cặp oxi hoá – khử Zn2+/Zn”. Hãy trình bày quan điểm của em về giả thuyết trên.
Câu trả lời tốt nhất
(a) Cấu tạo pin X: Điện cực Zn nhúng trong dung dịch Zn2+ 1M, điện cực Sn nhúng trong dung dịch Sn2+ 1M, hai dung dịch được nối với nhau bằng cầu muối.
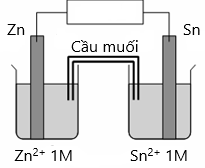
Cực âm (anode) Zn, cực dương (cathode) Zn.
Khi mạch ngoài kín sẽ có dòng electron di chuyển từ anode sang cathode —> Chiều dòng điện từ cathode sang anode.
Chú ý quy ước: Chiều dòng điện là chiều di chuyển của hạt mang điện dương. Nếu không có hạt mang điện dương thì chiều dòng điện ngược với chiều di chuyển của hạt mang điện âm.
(b) E°pin = E°Sn2+/Sn – E°Zn2+/Zn = 0,63V
(c)
ESn2+/Sn = E°Sn2+/Sn + ½.0,059.lg[Sn2+]
EZn2+/Zn = E°Zn2+/Zn + ½.0,059.lg[Zn2+]
Khi pin hết điện thì:
Epin = ESn2+/Sn – EZn2+/Zn = 0
⇔ E°Sn2+/Sn + ½.0,059.lg[Sn2+] = E°Zn2+/Zn + ½.0,059.lg[Zn2+]
⇔ lg[Zn2+] – lg[Sn2+] = 21,36
⇔ lg{[Zn2+]/[Sn2+]} = 21,36
⇔ [Zn2+]/[Sn2+]} = 10^21,36
(d)
Để có dòng điện, 2 điện cực phải có sự chênh lệch về điện thế. Theo phương trình Nernst, thế điện cực của Zn phụ thuộc vào nồng độ, vì vậy có thể thiết lập pin chỉ với điện cực Zn nhưng nồng độ Zn2+ ở 2 cốc phải khác nhau.
+ Điện cực Zn nhúng trong dung dịch Zn2+ có nồng độ lớn hơn sẽ có thế điện cực lớn hơn và là cực dương.
+ Điện cực Zn nhúng trong dung dịch Zn2+ có nồng độ nhỏ hơn sẽ có thế điện cực nhỏ hơn và là cực âm.
dạ thầy cho e hỏi công thức nernst ở câu c sao thầy k ghi log dạng khử của ct nernest
