Pin lithium–ion đã trở thành nguồn năng lượng chủ yếu cho các thiết bị điện tử di động ngày nay. Hơn thế nữa, nhờ những ưu điểm nổi bật so với các loại pin khác – đơn cử như mật độ lưu trữ năng lượng vượt trội – chúng đã mở đường cho sự phát triển của hàng loạt ứng dụng, vượt xa khỏi phạm vi công nghệ cốt lõi ban đầu, nổi bật là ứng dụng cho xe hybrid và xe điện.
Cấu tạo của pin: Điện cực iron phosphate (FePO4), ở ngăn 1 có khối lượng mFePO4 = 4,7 kg. Khi pin được sạc đầy, điện cực ở ngăn 2 được bao phủ bởi một lớp vật liệu carbon đã lithium hóa (công thức LiC6) nặng 1,1 kg. Các điện cực này được nhúng trong chất điện li hữu cơ dạng ion có chứa ion lithium và hai ngăn được phân cách bởi một màng ngăn.
– Để khởi động, chiếc xe ô tô cần điện lượng là qo = 45 Ah.
– Trong quá trình phóng điện của pin, các phản ứng hóa học tại các điện cực được mô tả như sau:
Giải phóng lithium tại ngăn 2:
LiC6(s) → 6C(s) + Li+(aq) + e
Hình thành lithium iron phosphate có công thức LiFePO4.
Li+(aq) + e + FePO4(s) → LiFePO4(s)
Một học sinh vẽ lại sơ đồ pin trong quá trình phóng điện như sau:
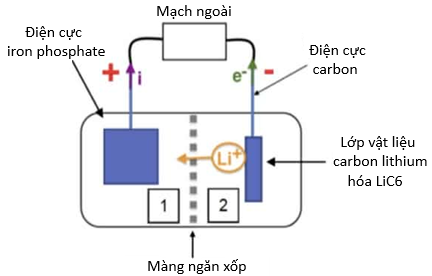
Cho biết: Điện lượng: q = ne.F. Trong đó: q là điện lượng (C), nc là số mol electron đi qua dây dẫn, F = 96485 C/mol, 1 C = 1 As.
a) Từ lúc bắt đầu cho đến lúc ngừng hoạt động pin đã cung cấp một điện lượng q gấp khoảng 18,5 lần điện lượng để khởi động xe là qo (làm tròn kết quả đến hàng phần mười).
b) Phương trình phản ứng tổng quát khi pin phóng điện: LiC6(s) + FePO4(s) → 6C(s) + LiFePO4(s).
c) Pin sẽ ngừng hoạt động khi sử dụng hết khoảng 14 mol LiC6(s) (làm tròn kết quả đến hàng đơn vị).
d) Sơ đồ pin đã được học sinh vẽ lại không chính xác.
Câu trả lời tốt nhất
(a) Sai:
nFePO4 = 4700/151 = 31,12583 mol
nLiC6 = 1100/79 = 13,92405 mol
Như vậy FePO4 dư và số mol electron tính theo LiC6.
—> ne = 13,92405 mol
q = ne.F = 1343462 As = 373,1839 Ah
Điện lượng này gấp 373,1839/45 = 8,3 lần điện lượng để khởi động xe.
(b) Đúng, gộp các quá trình điện cực lại ta có phản ứng:
LiC6(s) + FePO4(s) → 6C(s) + LiFePO4(s).
(c) Đúng, pin ngừng hoạt động khi LiC6 hết (do FePO4 dư), khi đó nLiC6 = 13,92405 ≈ 14 mol.
(d) Sai, sơ đồ này vẽ chính xác:
+ Electron di chuyển từ cực âm qua mạch ngoài đến cực dương. Chiều dòng điện ngược hướng với hạt mang điện âm nên di chuyển từ cực dương sang cực âm.
+ Li+ tạo ra từ bán phản ứng của ngăn 2 di chuyển sang ngăn 1 để tham gia bán phản ứng tại đây.

