Quá trình Solvay sản xuất Na2CO3 từ nguyên liệu chính đá vôi, muối ăn, ammonia và nước được mô tả bằng sơ đồ sau:
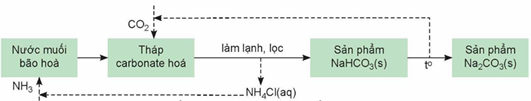
Phát biểu nào sau đây đúng?
A. Na2CO3(s) có thể được tạo thành trực tiếp bằng cách đun nóng hỗn hợp các nguyên liệu ban đầu.
B. NH4Cl được nhiệt phân để thu hồi NH3 đưa trở lại quá trình sản xuất.
C. Quy trình Solvay đã tái sử dụng các sản phẩm trung gian như NH3, CO2 qua đó giảm thiểu tác động đến môi trường.
D. Từ quy trình trên, ta thấy NaHCO3 kết tinh do có độ tan cao.
Câu trả lời tốt nhất
A. Sai, Na2CO3 có độ tan lớn nên không thể tách ra (nhất là khi đun nóng). Vì vậy cần làm lạnh để NaHCO3 (độ tan nhỏ, càng lạnh càng nhỏ) tách ra khỏi dung dịch, sau đó nhiệt phân NaHCO3 sẽ thu được Na2CO3.
B. Sai, không thể tách NH3 từ NH4Cl bằng con đường nhiệt phân (vì 2 khí NH3, HCl sẽ kết hợp với nhau ngay). Phải dùng CaO để tách NH3:
CaO + 2NH4Cl —> CaCl2 + 2NH3 + H2O
C. Đúng, đây là ưu thế của quy trình Solvay. Việc tái sử dụng CO2, NH3 vừa giúp giảm chi phí nguyên liệu, vừa giúp giảm thiểu tác động đến môi trường.
D. Sai, NaHCO3 kết tinh do có độ tan thấp (một chất chỉ kết tinh khi nồng độ của nó trong dung dịch bắt đầu vượt quá độ tan, nếu độ tan neo ở mức rất cao, sẽ rất khó để nó kết tinh).
