Tại 25°C, một pin điện hoá được thiết lập bởi một điện cực Ni nhúng trong dung dịch Ni(NO3)2 1,0M và một điện cực Cu nhúng trong dung dịch Cu(NO3)2 0,4M (mô tả như hình vẽ).
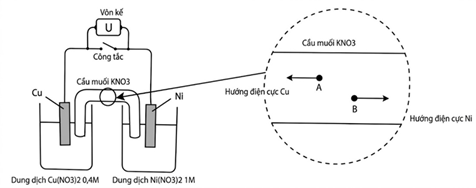
– Khi pin bắt đầu hoạt động, dưới tác dụng của điện trường trong dung dịch điện li, các ion A và B di chuyển ngược chiều nhau về các điện cực.
– Thế điện cực chuẩn của các cặp oxi hoá – khử như sau: E°Cu2+/Cu = +0,34 V và E°Ni2+/Ni = −0,257 V.
– Biết rằng thế điện cực của một cặp oxi hoá – khử ở nồng độ bất kì được tính theo phương trình Nernst: 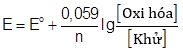
a. Khi giảm nồng độ ion kim loại trong dung dịch thì thế điện cực của kim loại không thay đổi.
b. Cu đóng vai trò là cực âm (anode), Ni đóng vai trò là cực dương (cathode).
c. Giá trị suất điện động của pin trên là: Epin = Ecathode − Eanode = 0,597 V.
d. A là cation K+ và B là anion NO3-.
Câu trả lời tốt nhất
(a) Sai, theo phương trình Nernst khi [oxi hóa] giảm thì E giảm.
(b) Sai, E°Cu2+/Cu > E°Ni2+/Ni nên Ni đóng vai trò là cực âm (anode), Cu đóng vai trò là cực dương (cathode).
(c) Sai:
Cu là chất rắn nên [khử] = 1, khi đó:
ECu2+/Cu = E°Cu2+/Cu + (0,059.lg0,4)/2 = 0,3283
ENi-Cu = ECu2+/Cu – E°Ni2+/Ni = 0,585V
(d) Đúng, Cu2+ bị khử nên K+ di chuyển tới thế chỗ Cu2+. Ni bị oxi hóa nên NO3- di chuyển tới kết hợp với Ni2+ mới giúp trung hòa điện tích.
