Cho 53,05 gam hỗn hợp gồm K, K2O, Ba, BaO vào nước dư, thu được V lít (đktc) khí H2 và dung dịch X. Sục 11,2 lít (đktc) khí CO2 vào dung dịch X thu được kết tủa và dung dịch Y. Cho rất từ từ dung dịch HCl 1M vào dung dịch Y, sự phụ thuộc của số mol khí CO2 thoát ra vào thể tích dung dịch HCl được biểu diễn theo đồ thị sau:
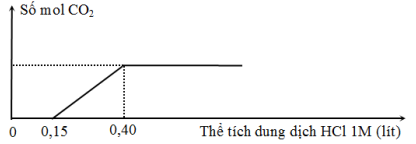
Giá trị của V là
A. 5,60. B. 10,08. C. 11,20. D. 6,72.
Câu trả lời tốt nhất
Y + HCl thoát ra nCO2 = 0,4 – 0,15 = 0,25
Ban đầu nCO2 = 0,5
Bảo toàn C —> nBaCO3 = 0,25
Do CO2 không thoát ra ngay (tốn 0,15 mol HCl mới bắt đầu thoát khí) nên Y chứa CO32- và OH- hoặc CO32- và HCO3- —> Y không chứa Ba2+.
Sau khi dùng hết 0,4 mol HCl thì dung dịch thu được chỉ có KCl (0,4)
—> Quy đổi hỗn hợp ban đầu thành Ba (0,25), K (0,4) —> nO = 0,2
Bảo toàn electron: 2nBa + nK = 2nO + 2nH2
—> nH2 = 0,25 —> V = 5,6 lít

