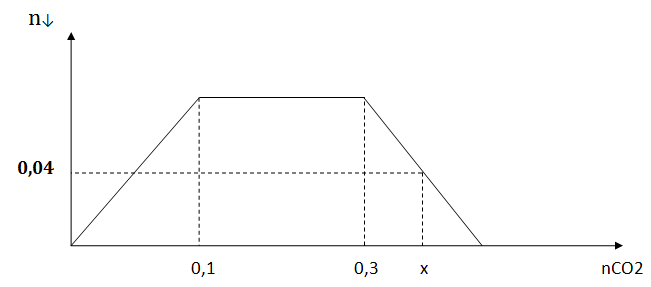
Đốt cháy hoàn toàn 0,18 mol hỗn hợp E gồm một anđehit và một hiđrocacbon (đều mạch hở, có số mol bằng nhau), thu được x mol CO2 và 0,18 mol H2O. Sục x mol CO2 vào dung dịch chứa hỗn hợp Ca(OH)2 và NaOH, kết quả thu được biểu diễn bằng đồ thị dưới đây:
Mặt khác, cho m gam E tác dụng với dung dịch AgNO3 dư trong NH3 (đun nóng), thu được 10,08 gam kết tủa. Giả trị của m là
A. 1,26. B. 2,64.
C.3,15. D. 7,56.
Câu trả lời tốt nhất
Khi nCO2 = 0,1 thì nCaCO3 max = 0,1
—> nCa(OH)2 = 0,1
Khi nCO2 = 0,3 thì kết tủa bắt đầu bị hòa tan —> nNaOH = 0,3 – 0,1 = 0,2 (Đoạn nằm ngang ứng với sự tạo thành NaHCO3)
Khi nCO2 = x thì nCaCO3 = 0,04
Bảo toàn Ca —> nCa(HCO3)2 = 0,06
Bảo toàn Na —> nNaHCO3 = 0,2
Bảo toàn C —> nCO2 = 0,04 + 0,06.2 + 0,2 = 0,36
—> x = 0,36
Số C = nCO2/nE = 2
Số H = 2nH2O/nE = 2
—> Cả 2 chất đều 2H. Do chúng có số mol bằng nhau nên loại trường hợp HCHO và C4H2.
—> E chứa (CHO)2 và C2H2 (0,09 mol mỗi chất)
—> mE = 7,56
Lượng E trên tạo ra Ag (0,36) và C2Ag2 (0,09)
—> m↓ = 60,48
Tỷ lệ:
7,56 gam E tạo ra 60,48 gam kết tủa
m gam E tạo ra 10,08 gam kết tủa
—> m = 10,08.7,56/60,48 = 1,26
Vi H trung bình bằng 2 và số mol bằng nhau nên 2 chất đều 2 H hạ anh vậy số C mỗi chất đều bằng 2 sao k đc hạ a

