Một anion X- có tổng số hạt là 53, trong đó số hạt mang điện chiếm 66,04%.
a. Xác định kí hiệu và tên gọi của nguyên tử X.
b. Lập công thức hợp chất khí với hiđro của X. Gọi tên hợp chất khí đó.
c. Cho hợp chất khí (nói trên) tan vào nước thu được dung dịch Y. Chỉ dùng dung dịch Y làm thuốc thử, hãy nhận biết bốn dung dịch riêng biệt sau: Na2CO3, Na2SO3, Na2SO4, Na2S. Viết phương trình hoá học của các phản ứng xảy ra (nếu có).
Câu trả lời tốt nhất
Số hạt mang điện = 2Z + 1 = 53.66,04%
—> Z = 17: X là Cl
Tổng hạt của X- = 2Z + N + 1 = 53 —> N = 18
A = Z + N = 35
Kí hiệu của X: 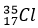
Hợp chất của X với hiđro là HCl (Hidro clorua)
Dùng dung dịch HCl để nhận biết:
+ Có khí không màu, không mùi là Na2CO3:
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
+ Có khí không màu, mùi hắc là Na2SO3:
Na2SO3 + 2HCl → 2NaCl + SO2 + H2O
+ Có khí không màu, mùi trứng thối là Na2S:
Na2S + 2HCl → 2NaCl + H2S
+ Không có khí là Na2SO4.
