Tiến hành điện phân 400 ml dung dịch chứa hỗn hợp CuSO4 aM và NaCl bM bằng dòng điện một chiều có cường độ không đổi, điện cực trơ, màng ngăn xốp. Mối liên hệ giữa giá trị pH của dung dịch và thời gian tiến hành điện phân được mô tả bằng đồ thị sau:
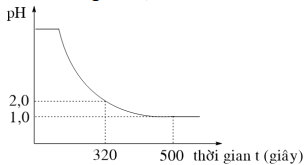
Từ thời điểm t = 500 giây trở đi, giá trị pH của dung dịch hầu như không thay đổi. Giả thiết thể tích dung dịch không thay đổi trong quá trình điện phân; hiệu suất quá trình điện phân là 100%; các chất HCl, NaOH, H2SO4 (cả 2 nấc) trong dung dịch điện ly hoàn toàn. Tổng (a + b) có giá trị là
A. 0,385. B. 0,275. C. 0,325. D. 0,425.
Câu trả lời tốt nhất
Đoạn đầu đồ thị nằm ngang do phản ứng:
CuSO4 + 2NaCl —> Cu + Cl2 + Na2SO4
Đoạn sau pH giảm dần do tạo ra axit nên phản ứng tiếp theo là:
CuSO4 + H2O —> Cu + ½O2 + H2SO4
Lúc t = 320s: pH = 2 —> [H+] = 0,01 —> nH+ = 0,004
Lúc t = 500s: pH = 1 —> [H+] = 0,1 —> nH+ = 0,04
—> Trong 180s (tính từ 320s đến 500s) phản ứng đã tạo ra thêm 0,04 – 0,004 = 0,036 mol H+
—> ne trong 180s = 0,036 —> ne trong 500s = 0,1
Từ thời điểm t = 500 giây trở đi, giá trị pH của dung dịch hầu như không thay đổi do H2O bắt đầu điện phân ở cả 2 điện cực.
nCuSO4 = 0,4a; nNaCl = 0,4b, trong 500s đầu tiên:
Catot: nCu = 0,4a = 0,1/2 —> a = 0,125
Anot: nO2 = nH+(500s)/4 = 0,01 —> nCl2 = 0,03
—> nNaCl = 0,4b = 0,06 —> b = 0,15
—> a + b = 0,275
