Điện phân dung dịch chứa Cu(NO3)2, CuSO4 và NaCl với điện cực trơ, cường độ dòng điện không đổi 5A hiêu suất 100%. Kết quả thí nghiệm được ghi trong bảng sau
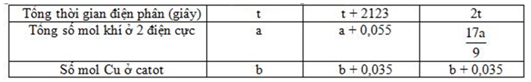
Giá trị của t là
A. 1158 B. 1544 C. 1737 D. 2316
Câu trả lời tốt nhất
Trong khoảng thời gian 2123 (s) (trao đổi 0,11 mol electron) thì tại cực âm thoát ra 0,035 mol Cu, bảo toàn electron —> nH2 = 0,02
—> 0,055 mol khí gồm H2 (0,02), Cl2 (x mol) và O2 (y mol)
—> x + y + 0,02 = 0,055 và 2x + 4y = 0,11
—> x = 0,015 và y = 0,02
Trong khoảng thời gian từ t + 2123 —> 2t chỉ là điện phân H2O nên phần khí tăng thêm là 17a/9 – (a + 0,055) = 8a/9 – 0,055 chỉ bao gồm O2 và H2. Do nH2 = 2nO2 nên:
nO2 = 8a/27 – 0,055/3
Như vậy trong thời gian từ t —> 2t thì tại cực dương có:
nCl2 = 0,015
nO2 = 8a/27 – 0,055/3 + 0,02
Bảo toàn electron cho cực dương ở 2 khoảng thời gian (0 —> t) và (t —> 2t)
2a = 0,015.2 + 4(8a/27 – 0,055/3 + 0,02)
—> a = 0,045
Do a = It/2F —> t = 1737s
Tại sao trong khoảng thời gian từ t=>2t thì lại không tính ne trao đổi của H2 vậy ạ ???
