Một học sinh thực hiện quá trình điện phân nối tiếp dung dịch AgNO3 và Fe(NO3)2 bằng các điện cực platin, cường độ dòng điện 2A như hình bên.
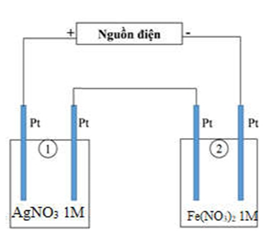
– Bình (1) chứa 200 ml dung dịch AgNO3 1M.
– Bình (2) chứa 300 ml dung dịch Fe(NO3)2 1M.
Sau thời gian t (giây), học sinh quan sát thấy có 8,4 gam kim loại sắt bám lên điệc cực của bình (2). Biết trong hệ điện phân nối tiếp, số electron truyền dẫn trong các bình là như nhau.
Cho các mệnh đề sau:
(1) Thời gian điện phân t = 9650 (giây).
(2) Sau t (giây), khối lượng kim loại Ag bám trên điện cực ở bình (1) là 64,8 gam.
(3) Sau 14475 (giây) thì khí bắt đầu thoát ra tại anot của bình (1).
(4) Sau thời gian 2t (giây), tổng thể tích khí thoát ra ở các điện cực của hai bình là 11,2 lít (đktc).
(5) Trong quá trình điện phân, pH của dung dịch trong hai bình luôn giảm.
Số mệnh đề đúng là
A. 1. B. 2. C. 3. D. 4.
Câu trả lời tốt nhất
Ban đầu: nAgNO3 = 0,2; nFe(NO3)2 = 0,3
(1) Sai: nFe = 0,15 = It/2F —> t = 14475s
(2) Sai, ne = 2nFe = 0,3 > nAg+ —> Ag+ đã bị điện phân hết và mAg = 0,2.108 = 21,6 gam
(3) Sai, anot bình 1 có O2 thoát ra ngay từ đầu.
(4) Đúng
ne trong 2t giây = 0,15.2.2 = 0,6
Bình 1: nAg = 0,2; nH2 = 0,2; nO2 = 0,15
Bình 2: nFe = 0,3; nO2 = 0,15
—> n khí tổng = 0,5 —> V = 11,2 lít
(5) Đúng, khi điện phân các muối có tạo axit nên pH giảm. Khi các muối bị điện phân hết, nước bị điện phân ở hai điện cực làm nồng độ axit tăng dần nên pH giảm.
Mn cho e hỏi là khi điện phân hết Ag+ thì Cathode ở bình 1 và Anode ở bình 2 còn hoạt động nữa kh ạ
